|
|
 发表于 2018-6-13 22:28:29
|
发表于 2018-6-13 22:28:29
|
查看: 106895 |
回复: 4
文章导读:长期以来,古人类女性骨盆演化都被解释成对直立行走和分娩机制的响应,而很少人关注经常性面对面交配对女性骨盆的作用,这种体位在类人猿中也有发现。本文根据前人重建的各古人物种女性骨盆,并与现存灵长动物雌性个体骨盆形状及分娩机制进行类比,探讨了自早期祖先与大猩猩分化以来的女性骨盆和分娩机制演化趋势。研究认为,早期女性骨盆演化主要受到面对面交配体位的影响,骨盆形状从矢向卵形向横向扁平卵形转变。伴随着越来越灵活的髋臼关节,直立行走出现并成为影响女性骨盆演化的主导因素,中骨盆又从横向扁平卵形转变为矢向卵形;耻骨则更多地承受面对面交配的作用力,骨盆入口继续维持横向扁平卵形的水平,最终形成现代女性特殊的“扭曲”的骨盆形状。直立行走等起源之谜的解答也可以从中得到启示。
关键词:女性骨盆演化 分娩 面对面交配 直立行走 灵长动物 古人类
1 引言
自赫胥黎[1]以来,骨盆演化经常被用来解释对直立行走的适应[2-6]。与此同时,Schultz[7]、Krogman[8]、Washburn[9]等也很关注现存灵长动物骨盆形状对分娩机制的制约。直到Sts-14、AL288-1等骨盆骨化石的相继发现,学者们才得以重建古人类女性骨盆形状及分娩机制,主要代表有Robinson[3]、Leutenegger[10][11]、Lovejoy[4]、Schimd[12]、Berge等[13][14]、Tague等[15]、Trevathan[16]、Abitbol[17] [18]、Husler等[19]。
Lovejoy[20]最近指出,更新世以来,女性骨盆演化主要受到分娩具更大头颅胎儿影响。而新发现的南方古猿源泉种(Australopithecus sediba)[21]化石证据似乎不太支持他的观点,NH2髋骨、骶骨等形态特征以及据此重建的骨盆形状都显示,尽管可通过的胎儿头颅尺寸可能没有明显增大,但与后期人属(如直立人Homo erect)类似的一些解剖性状已经出现[22]。另外,晚期尼安德特人(Homo neanderthalensis)成年个体头颅很大,甚至超过了直立人和现代智人(Homo sapiens)[23],其幼体头颅也可能很大,但Weaver等[24]重建的Tabun骨盆形状却类似于更早的南方古猿(如AL288-1)。
关于进化早期,Lovejoy[20]则强调直立(行走)姿势的影响。撒海尔人乍得种(Sahelanthropus tchadensis)枕骨大孔前置[2] [26],原初人图根种(Orrorin tugenensis)有别于现存猿和人、而与南方古猿更类似的股骨特征[27] [28],都对已有关于直立行走起源时间和演化进程的认识提出了更多新的挑战。正如Richmond等[28]所言,早期人类演化可能经历了一个复杂的过程,直到晚上新世早期人属(Homo)的出现。
面对面的交配体位同样也是现代人独特的行为方式之一。但已发现长臂猿 [29-31]、红毛猩猩[32-33]、大猩猩[33-34]、波诺波猿(Pan paniscus,又称“倭黑猩猩”)[35-39]等也会采用面对面的体位,青春期波诺波猿更是对这一体位偏爱有加,根据Blount[40]的统计,青春期波诺波猿已在近75%的交配行为中采用了这种体位,这暗示了早期祖先面对面交配的可能。频繁采用面对面体位可能会给骨盆带来戏剧性的变化,直立行走等起源也可能与之有关,但研究古人类女性骨盆演化的学者们却很少关注这一点。
2 现存灵长动物分娩制约
一般认为,非人灵长动物分娩的主要约束来自骨盆入口[7] [16] [41] [42]。Tague等[43]已发现了中骨盘对胎儿头颅的重要制约作用,但没能进一步分析中骨盆是如何制约胎儿肩宽的。Trevathan等[42]评述道,肩膀对分娩制约的重要性可能被低估了。
为了更好地分析不同肩宽对分娩机制的约束,这里将新生儿的体型划分为三种类型:窄肩型、宽肩型和过渡型(参见表1)。
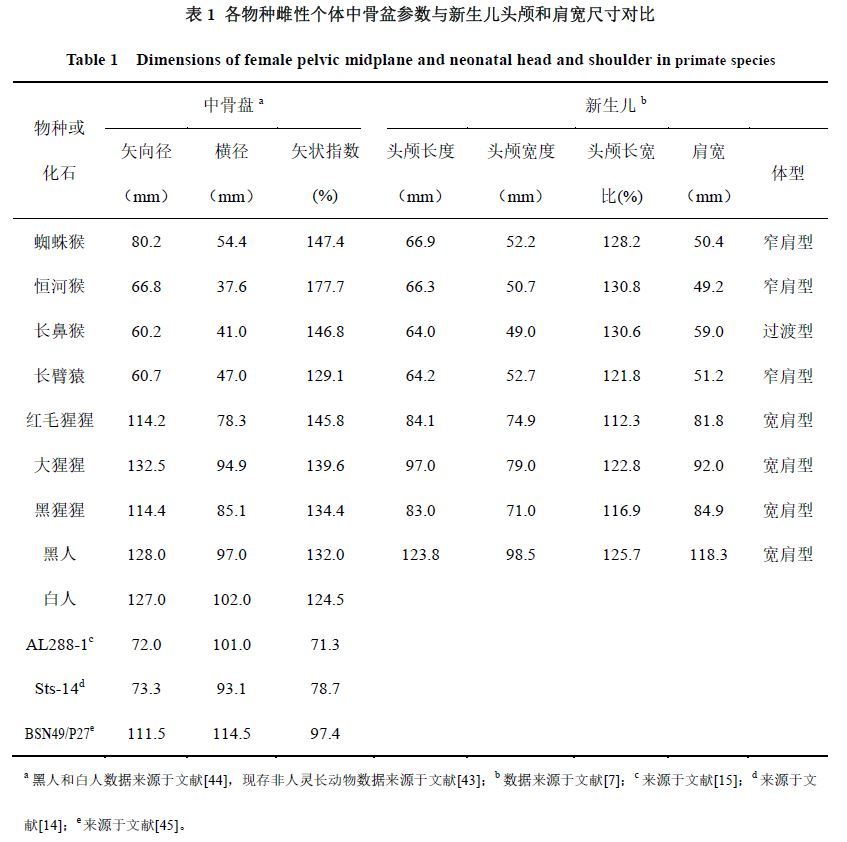
窄肩型指的是新生儿的肩部宽度小于头颅宽度,如蜘蛛猴(Ateles geoffroyi)、恒河猴(Macaca mulatta)和长臂猿(Hylobates lar)。这种体型的双肩对分娩几乎不构成影响,只要头部能顺利娩出,肩部和躯体顺利娩出是很自然的事(如蜘蛛猴)。然而,雌性恒河猴和长臂猿的中骨盘横径明显小于需分娩头颅的宽度,致使分娩也不是件容易的事。尤其是恒河猴,中骨盘横径均值仅为37.6毫米,而胎儿头颅宽度为中骨盆横径的1.348倍,达50.7毫米,可能是造成该物种分娩相对困难,耗时也相对较多的原因[41]。参见图1。
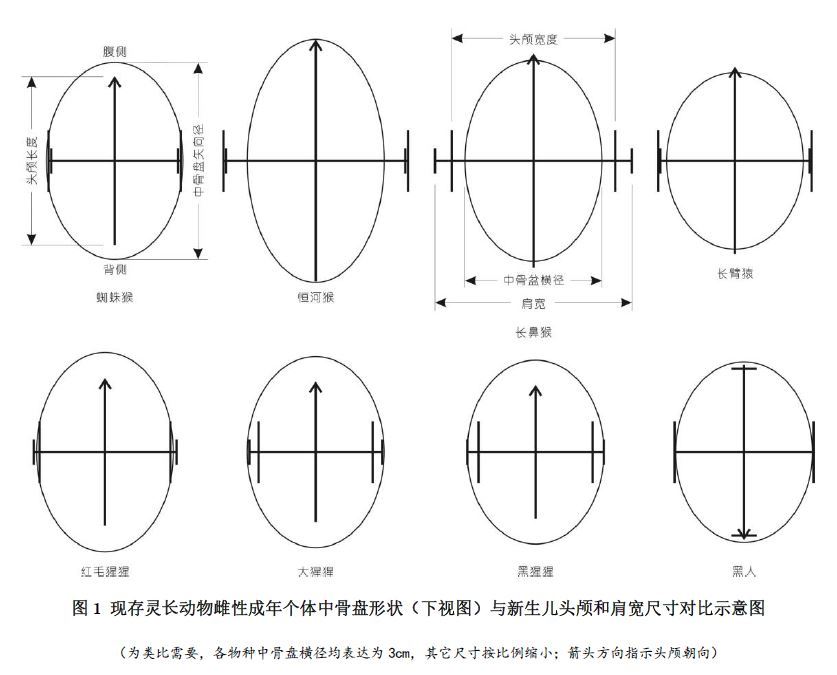
宽肩型指的是新生儿的肩部宽度明显大于头颅宽度,Schultz[7]提供的数据显示,大猿和现代智人新生儿的肩部宽度与头颅长度非常接近,除新生黑猩猩(Pan troglodytes)肩部宽度略大于头颅长度外,红毛猩猩(Pongo pygmaeus)、大猩猩(Gorilla gorilla)和现代智人新生儿的肩部宽度都略小于头颅长度。圆形应该是这些物种比较理想的产道形状。
从大猿雌性个体中骨盘参数来看,其横径与新生儿肩部宽度相当,分娩相对轻松。这和前人[7] [41]研究结果比较一致。Schultz[7]用新生儿与骨盆入口对比的结果显示,骨盆四周似乎有很大的“剩余空间”。而与中骨盆对比的结果则不同,除矢向上还有一定“剩余空间”外,横向上几乎没有“剩余空间”(图1)。这个结果表明,中骨盆横径仍是大猿母体娩出胎儿的制约因素之一。
相对于现存猿猴,现代人的分娩机制则要复杂得多[7] [16] [41]。但如果仅从胎儿以何种姿势通过中骨盘来看,可简单表述为:确保尺寸较大的头颅长度和肩部宽度与骨盆腔长轴保持一致。由于头盘不对称等因素,胎儿只有通过旋转才能娩出产道,是一种非常特殊的分娩方式。除头部较难娩出外,较宽的肩部也可能引发难产[46]。
在窄肩与宽肩之间,存在一种过渡类型,其肩部宽度介于头颅长度和头颅宽度之间,如长鼻猴(Nasalis larvatus)。其分娩方式大致与大猿一致,除头颅难娩出外,肩部也是一种制约。而长鼻猴母体相对较窄的中骨盘横径会造成分娩的困难,这是不是也是该物种面临灭绝风险的原因之一呢?
尽管不同物种新生儿体型存在较大差异,头部形状的差异却很小。定量化的长宽比也体现了这种特征,其比值介于112.3%(红毛猩猩)和130.8%(恒河猴)之间,平均值为123.3%。由此可见,在肩部变化较大的演化进程中,头部的变化相对较少。可能是肩部骨骼相对脆弱,易于改变;而头部骨骼相对坚硬,较难改变的原因。人类演化也应该遵循这一规律。
进一步分析可知,新大陆猴(如蜘蛛猴)和旧大陆猴(如恒河猴、长鼻猴)新生儿头颅长宽比均值都大于125%,而类人猿(包括长臂猿、红毛猩猩、大猩猩和黑猩猩)都小于125%,黑人头颅长宽比最接近这一比值,为125.7%。白人女性中骨盘矢状指数也非常接近这个值,为124.5%(表1)。这一比值的发现应归功于现代人类起源论的先驱赫胥黎先生,他曾用这一比值(即100:80,转换为百分比刚好是125%)来区分长头型人(oblong)和短头型人(dolichocephalic)[1]。为此,将125%的头颅长宽比称为“赫胥黎比”。有理由假设,自共同祖先以来,新生儿的头颅长宽比应比较接近这个值,不应该偏离太多。
3 古人类女性骨盆及其分娩
3.1 从Lucy到尼安德特人
Lucy(AL288-1)的分娩方式也是最具争议的问题之一。最广为接受的是胎儿以横向姿势通过所谓“极度横向扁平卵形”的产道[11][15][17][41][47]。尽管Lovejoy[4]构建的骨盆形状与现存猿类和现代智人都具有较大差别,但仅从绝对尺寸来看,与新生大猩猩同等大小的胎儿头颅应能通过Lucy的骨盆(参见表1)。中骨盆矢向径(72mm)只是略小于新生儿头颅宽度(79mm),横向通过时,头颅两侧受到一定约束,这种约束在现存灵长动物中都是存在的。如果不考虑头颅朝向,与长臂猿等分娩方式可以类比。
Trevathan[16]假设南方古猿阿法种新生儿与现代智人一样,也具有宽阔而坚硬的双肩,肩部必须旋转以适应极度横向扁平卵形的产道。而我认为,比头颅更易于改变的肩部,在骨盆矢向极度压缩的情况下,肩部宽度可能相应地减小,甚至返祖到长臂猿的体型,即窄肩型。南方古猿阿法种成年个体相对较小也可能是窄肩型胎儿引起。如果真是这样,肩部和躯体不旋转也可以顺利娩出。
根据Berge等[14]最近重建的南方古猿非洲种Sts-14骨盆形状参数,与新生大猩猩同等大小的胎儿头颅也应该可以通过Sts-14的骨盆(参见表1),中骨盆横径(93.1mm)和矢向径(73.3mm)都只是略小于头颅长度(97mm)和头颅宽度(79mm),但两个方向上都受到一定的制约。中骨盘矢状指数为78.7%,非常接近赫胥黎比倒数(80%)。可以推测,经历极度横向扁平卵形后,矢向上的约束有所释放,新生儿可能出现了从窄肩到宽肩的过渡类型,即类似于长鼻猴的过渡型。
直立人BSN49/P27的中骨盘形状接近圆形[45],其矢状指数为97.4%,非常有利于分娩宽肩型幼体,胎儿肩部得到充分发展可能也是造成该物种体形较大的原因之一。需要指出的是,圆形是骨盆从横向扁平卵形向矢向卵形过渡的形状。横向扁平卵形有利于胎儿横向通过,矢向卵形则有利于胎儿矢向通过,因此,也是分娩方式的“分水岭”。
据报道,最近发现的南方古猿源泉种,NH2中骨盘形状已经向所谓更“女性化”的形状转变[22],但其尺寸大小与AL288-1和Sts-14接近,明显小于BSN49/P27(参见表1)。年龄数据(~1.977—1.98Ma)[48]与直立人开始出现的时间(~2.0Ma)[49]比较一致,体现了南方古猿到直立人过渡的特点,能娩出的新生儿体形比直立人要小。
Weaver等[24]最近重建了尼安德特人Tabun的骨盆。骨盆入口和出口的矢状指数分别为79%和70%,中骨盘也是横向扁平卵形的,具有类似于南方古猿(特别是阿法种)的解剖性状,分娩方式应该没有太大差别。其成年个体头颅大于直立人和现代人[23],身材却明显矮小[50],很有可能是与南方古猿阿法种类似的窄肩型胎儿引起。
3.2 从共同祖先到Lucy
根据Lucy以来的古人类女性骨盆演化及其与现存猿猴的对比,可以假设,从共同祖先到Lucy,女性骨盆发生了类似的逐渐演化的过程。不同的是,从共同祖先到Lucy,中骨盆形状从矢向卵形(如大猿)向极度横向扁平卵形(如AL288-1)演化,而继Lucy之后,中骨盆又从极度扁平卵形向矢向卵形(如现代智人)转化。进一步假设,矢状指数在接近或跨越125%(赫胥黎比)、100%(圆形)和80%(赫胥黎比倒数)时,新生儿肩宽和体型发生相应的变化。
根据这样的假设,自与大猩猩分化以来,人类分支的进化大致经历了8个阶段,南方古猿阿法种相当于第五个阶段物种(H5),南方古猿非洲种、直立人和智人分别为第六、第七和第八个阶段物种(H6、H7和H8)(参见图2)。
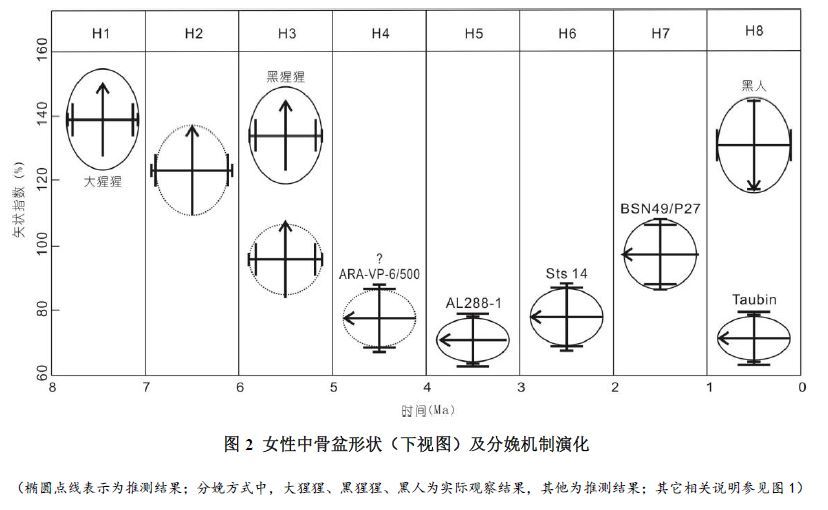
以H5为分界点,第四个阶段H4的骨盆形状大致与第六个阶段H6的相当,中骨盆矢状指数也应该接近赫胥黎比倒数(80%)。其时间上与地猿始祖种(Ardipithecus ramidus)[51]一致,根据Lovejoy等[6]重建的ARA-VP-6/500骨盆形状,矢状指数应该出入不大。推测新生儿体型为过渡型。
第三个阶段H3(如原初人图根种)则与第七个阶段H7大致相当。虽然缺少可对比的早期圆形骨盆,但图根种(BAR-1002′00)比黑猩猩更加粗壮的股骨体和股骨头表明具有较大个体[28],可能与圆形(或近圆形)骨盆有利于分娩更大的宽肩型胎儿有关,相对较长的股骨颈[28]则指示骨盆从矢向卵形到横向拓展的可能。
第二个阶段H2(如撒海尔人乍得种)则与第八个阶段(H8)现代智人相当,正如以上分析,白人女性的中骨盘参数非常接近赫胥黎比(125%)。从中骨盘矢向上有较多的“剩余空间”(如H1),到几乎无“剩余空间”是这个阶段物种分娩的特点。乍得种(TM266)枕骨大孔前置[25] [26],有利于胎儿在脑前后部都受到约束的情况下,从中部使力娩出。这与Stoller[52]观察到的狒狒(Papio anubis)和松鼠猴(Saimiri sciureus)昂头、脸先娩出的机制具有同样的效果。
现代人祖先和黑猩猩可能在这个阶段晚期发生分化,矢向上的进一步压缩可能引起新生儿头颅尺寸变小,形成了成年个体也相对较小的黑猩猩一支。而新生儿头颅未变小的另一个分支,则由于圆形中骨盆的出现,胎儿肩部得到充分发展。雌性黑猩猩中骨盘矢状指数均值(134.4%)大于125%(赫胥黎比),其下限值也未达到圆形水平(100%)[43]。
至于第一阶段H1,未发现可靠的化石证据,推测女性骨盆形状、新生儿体型和分娩方式都与现生大猩猩类似,中骨盆矢向上有较多的“剩余空间”是该阶段物种分娩的主要特点(请参见大猩猩的分娩机制,这里不再赘述)。
4 讨论
4.1 进化方向及例外
图2绘制了现代人进化分支女性骨盆及分娩机制的演化趋势。从总体上看,从H1到H5,新生儿体型有逐渐被压缩的趋势,成年个体逐渐变小,南方古猿阿法种是已发现体形最小的古人物种之一。而继H5之后,伴随着中骨盆矢向径的不断扩大,新生儿头颅有逐渐增大的趋势,成年个体也相应变大。直立人、傍人(Paranthropus)等更新世物种,体形明显偏大。
不能否认的是,很多物种并未按照这样的路线演化,就像大猩猩和黑猩猩一样,仍然保留着更多早期的性状。一个比较典型的例子可能是肯尼亚平脸人(Kenyanthropus platyops)[53],时间上与南方古猿阿法种重叠,可以推测具有与AL288-1类似的骨盆形状,如果其分娩方式未发生改变,胎儿仍然是以头颅矢向通过产道的话,耻骨联合与骶骨之间较短的矢向径会强烈挤压胎儿头颅前后部,可能引起成年后呈现扁平的面部轮廓。
另一个典型的代表是尼安德特人,作为现代智人即将出现之前的相对较晚的智人物种,却继承了南方古猿的骨盆形状,骨盆入口、中骨盆和骨盆出口都是横向扁平卵形的[24]。其较短的胫骨和腓骨、宽阔的胸腔、较长的锁骨等性状[50],说明该物种并不像直立人和现代智人那样适应长时间直立行走,特别是持续跑,可能是骨盆形状未向圆形或矢向卵形转变的原因。
4.2 演化进程与分子钟
从前人重建各物种的骨盆形状及其演化过程来看,从前一个阶段的骨盆形状到下一阶段的骨盆形状出现,如从南方古猿阿法种到非洲种出现、从非洲种到直立人出现、从直立人再到智人出现,大致都经历了100万年左右的时间[49]。有理由假设,自早期祖先与大猩猩分化以来,每一个阶段都经历了大约100万年左右的时间,8个阶段就是800万年,这与线粒体DNA对比的结果比较一致,推测和黑猩猩分家的时间(约600万年前)也是如此(参见图2)[54]。
在每一个时间节点上,最有可能发生新物种的诞生或旧物种的灭亡。在骨盆不断变化的过程中,部分个体通过分娩机制或胎儿体型的改变,实现了到新物种的进化。另一些未进行改变的个体,则可能继续维持已有的状态,某些持续的行为方式还可能引起骨盆的极度异化,最终导致分娩的困难或极度困难。如果上述理论成立,或许可以作为所谓“分子钟”的形态学解释。
4.3 面对面交配起因解释
不能回避的是“为什么”的问题,也就是什么原因促使这种演化发生的问题。
在前人研究古人类骨盆及分娩方式演化的过程中,除了直立行走和分娩胎儿外,有一个经常作用于女性骨盆的外力可能被学者们所忽视,那就是面对面的交配姿势。在传统男上女下的体位中,来自男性伴侣抽动阴茎的作用力和身体自重都可能使女性骨盆矢向上受到挤压,横向伸展则是矢向挤压引起的侧向挤出效应,还有可能包括来自股骨头的直接牵引。
面对面交配也是现代人特有的行为方式之一,在类人猿中也有发现[29-39],但仍存在较大差别。身体相对灵活的青春期波诺波猿,已在75%的交配活动中采用了面对面的交配姿势[40],这暗示了早期祖先面对面交配是非常有可能的。如果采用这种体位更加频繁,可能会带来意想不到的变化。
古人类女性骨盆相对较大的耻骨下角[14] [15] [24] [45],使阴道口前置成为可能,更有利于阴茎从前方插入,就象现代人一样。雌性波诺波猿等阴道口相对后置,插入方式一定程度上仍然可以称作是“后入式”的,尽管彼此都是面朝对方。这也是不同于现代人面对面体位的主要特征之一。
AL288-1等向内侧弯曲的股骨体[5],有利于在面对面的交配过程中用脚“拥抱”伴侣身体,这种“拥抱”姿势在现存猿和现代人中都有发现。这种拥抱姿势可能会使“拉弯”股骨体、“拉长”股骨颈,股骨颈上薄下厚的皮质层骨也可能与这种“拉弯”效应有关。这些性状在原初人图根种股骨中已有发现[28]。
综合以上分析,早期人类演化可能主要受到面对面交配的影响,女性骨盆形状从矢向卵形向横向扁平卵形转变。频繁的面对面体位使得髋臼关节等越来越灵活,也促成了直立(行走)姿势。晚期则主要受到直立行走的影响,在左右两侧股骨头向内侧的挤压作用下,中骨盆又从横向扁平卵形转变成了矢向卵形;耻骨仍然受到面对面体位的强烈作用,骨盆入口仍然是横向扁平卵形的。至此,“扭曲”的骨盆形状最终形成。
5 结论
本文根据前人重建的各古人物种女性骨盆形状,并与现存灵长动物骨盆形状、分娩方式等类比,探讨了自早期祖先与大猩猩分化以来的骨盆演化趋势。很多设想都是初步的,一些细节仍有待于进一步深化,更有待于更多新的化石证据提供佐证。但中骨盆先从矢向卵形到横向扁平卵形,而后又变成矢向卵形的逐渐演化的过程却是比较清晰的。在此基础上提出,面对面交配可能引起了早期物种女性骨盆的演化,后期则主要受到直立行走的影响。直立行走等起源之谜的解答也可以从中得到启示。
参考文献(References):
[1] Huxley T H. Evidence as to Man's place in nature [M]. London: Williams & Norgate, 1863.
[2] Dart R A. The first pelvic bones of Australopithecus prometheus: preliminary note [J]. Am. J. Phys. Anthropol., 1949, 7:255-257.
[3] Robinson J T. Early Hominid Posture and Locomotion [M]. Chicago: University of Chicago Press, 1972.
[4] Lovejoy C O. A reconstruction of the pelvis of AL288-1 (Hadar formation, Ethiopia) (Abstract) [J]. Am. J. Phys. Anthropol. Suppl., 1979, 50: 460.
[5] Lovejoy C O, Meindl R S, Ohman J C, et al. The Maka femur and its bearing on the antiquity of human walking: applying contemporary concepts of morphogenesis to the human fossil record [J]. Am. J. Phys. Anthropol., 2002, 119: 97-133.
[6] Lovejoy C O, Suwa G, Spurlock L, et al. The pelvis and femur of Ardipithecus ramidus: the emergence of upright walking [J]. Science, 2009, 326: 71e1-71e6.
[7] Schultz A H. Sex differences in the pelves of primates [J]. Am. J. Phys. Anthropol., 1949, 7: 401-424.
[8] Krogman W M. The scars of human evolution [J]. Sci. Amer., 1951, 185, 54-57.
[9] Washburn S L. Tools and human evolution [J]. Sci. Amer., 1960, 203(3): 3-15.
[10] Leutenegger W. Newborn size and pelvic dimensions of Australopithecus [J]. Nature, 1972, 240: 568-569.
[11] Leutenegger W. Neonatal brain size and neurocranial dimensions in Pliocene hominids: implications for obstetrics [J]. J. Hum. Evol., 1987, 16: 291-296.
[12] Schmid P. Eine Rekonstruktion des Skelettes von A.L.288-1 (Hadar) und deren Konsequenzen [J]. Folia. Primatol., 1983, 40: 283-306.
[13] Berge C, Orban-Segebarth R, Schmid P. Obstetrical interpretation of the australopithecine pelvic cavity [J]. J. Hum. Evol., 1984, 13: 573-587.
[14] Berge C, Goularas D. A new reconstruction of Sts 14 pelvis (Australopithecus africanus) from computed tomography and three-dimensional modeling techniques [J]. J. Hum. Evol., 2010, 58: 262-272.
[15] Tague R G, Lovejoy C O. The obstetric pelvis of A.L. 288-1 (Lucy) [J]. J. Hum. Evol., 1986, 15: 237-255.
[16] Trevathan W. Fetal emergence patterns in evolutionary perspective [J]. Am. Anthropol., 1988, 90: 674-681.
[17] Abitbol M M. Ontogeny and evolution of pelvic diameters in anthropoid primates and in Australopithecus Afarensis (AL 288-1) [J]. Am. J. phys. Anthrop., 1991, 85: 135-148.
[18] Abitbol M M. Reconstruction of the STS 14 (Australopithecus africanus) pelvis [J]. Am. J. phys. Anthrop., 1995, 96: 143-158.
[19] Husler M, Schmid P. Comparison of the pelves of Sts 14 and A.L. 288-1: implications for birth and sexual dimorphism in australopithecines [J]. J. Hum. Evol., 1995, 29: 363-383.
[20] Lovejoy C O. The natural history of human gait and posture part 1. Spine and pelvis [J]. Gait and posture, 2005, 21: 95-112.
[21] Berger L R, J de Ruiter D, Churchill S E, et al. Australopithecus sediba: A new species of Homo-like australopith from South Africa [J]. Science, 2010, 328: 195-204.
[22] Kibii J M, Churchill S E, Schmid P, et al. A partial pelvis of Australopithecus sediba [J]. Science, 2011, 333: 1407-1411.
[23] Zollikofer C P E, Pance de Leon M S. The evolution of hominin ontogenies [J]. Seminars in Cell & Developmental Biology, 2010, 21: 441-452.
[24] Weaver D T, Hublin J-J. Neanderthal birth canal shape and the evolution of human childbirth [J]. Proc. Natl. Acad. Sci. USA, 2009, 106: 8151-8156.
[25] Brunet M, Guy F, Pilbeam D, et al. A new hominid from Upper Miocene of Chad, Central Africa [J]. Nature, 2002, 418: 145-151.
[26] Zollikofer C P E, Ponce de Leon M S, Lieberman D E, et al. Virtual cranial reconstruction of Sahelanthropus tchadensis [J]. Nature, 2005, 434: 755-759.
[27] Senut B, Pickford M, Gommery D, et al. First Hominid from the Miocene (Lukeino Formation, Kenya) [J]. C. R. Acad. Sci. Paris, 2001, 332: 137-144.
[28] Richmond B G, Jungers W L. Orrorin tugenensis femoral morphology and the evolution of hominin bipedalism [J]. Science, 2008, 319: 1662-1665.
[29] Koyama N. Observations on mating behavior of wild siamang gibbons at Fraser’s Hill, Malaysia[J]. Primate, 1971, 12(2):183-189.
[30] 杨梅. 白眉长臂猿在人工饲养条件下的交配行为[J]. 野生动物, 1998, 19(1): 33.
[31] 潘阳. 笼养白眉长臂猿的繁殖初探[J]. 四川动物, 2000, 19(2): 88-89.
[32] Fox H. The birth of two anthropoid apes[J]. Journal of Mammalogy, 1929, 10(1): 37-51.
[33] Nadler R D. Sexual behavior of captive orangutans[J]. Archives of sexual behavior, 1977, 6(6): 457-475.
[34] Schaller G B. The Mountain Gorilla: ecology and behavior[M]. Chicago: University of Chicago Press, 1963.
[35] Nadler R D. Sexual behavior of captive lowland gorillas[J]. Archives of sexual behavior, 1976, 5(5): 487-502.
[36] Savage-Rumbaug E S, Wilkerso B J. Socio-sexual behavior in pan paniscus and pan troglodytes: a comparative study[J]. Journal of human evolution, 1978, 7(4): 327-344.
[37] Patterson T. The behavior of a group of captive pygmy chimpanzees (pan paniscus)[J]. Primates, 1979, 20(3): 341-354.
[38] McHenry H M, Corruccini R S. Pan paniscus and human evolution[J]. American journal of physical anthropology, 1981, 54(3): 355-367.
[39] Dahl J F. The external genitalia of female pygmy chimpanzees[J]. The anatomical record, 1985, 211(1): 24-28.
[40] Blount B G. Issues in bonobo (Pan paniscus) sexual behavior[J]. American anthropologist, 1990, 92(3): 702-714.
[41] Rosenberg K. The evolution of the modern childbirth [J]. Yearb. Phys. Anthropol., 1992, 35: 85-124.
[42] Trevathan W, Rosenberg K. The shoulders follow the head: postcranial constraints on human childbirth [J]. J. Hum. Evol., 2000, 39: 583-586.
[43] Tague R G, Lovejoy C O. AL 288-1 Lucy or Lucifer: gender confusion in the Pliocene [J]. J. Hum. Evol., 1998, 35: 75-94.
[44] Tague R G. Variation in pelvic size between males and females [J]. Am. J. Phys. Anthropol., 1989, 80: 59-71.
[45] Simpson S W, Quade J, Levin N E, et al. A female Homo erectus pelvis from Gona, Ethiopia [J]. Science, 2008, 322: 1089-1092.
[46] Smeltzer J S. Prevention and management of shoulder dystocia [J]. Clin. Obst. Gynecol., 1986, 29: 299-308.
[47] Ruff C B. Biomechanics of the hip and birth in early Homo [J]. Am. J. Phys. Anthropol., 1995, 98: 527–574.
[48] Pickering R, Dirks P H, Jinnah Z, et al. Australopithecus sediba at 1.977 Ma and implications for the origins of the genus Homo [J]. Science, 2011, 333: 1421-1423.
[49] Wood B, Lonergan N. The hominin fossil record: taxa, grades and clades [J]. J. Anat., 2008, 221: 354-376.
[50] Stringer C, Andrews P. The complete world of human evolution (2nd ed.) [M]. London: Thames and Hudson, 2011.
[51] White T D, Suwa G, Asfaw B. Australopithecus ramidus, a new species of early hominid from Aramis, Ethiopia [J]. Nature, 1994, 371: 306-312.
[52] Stoller M. The obstetric pelvis and mechanism of labor in nonhuman primates [D]. Ph.D. Dissertation, University of Chicago, 1995.
[53] Leakey L N, McDaugall I. New hominin genus from eastern Africa shows diverse middle Pliocene lineages [J]. Nature, 2001, 410: 433-440.
[54] Marques-Bonet T, Ryder O A, Eichler E E. Sequencing primate genomes: what have we learned [J]? Annu. Rev. Genomics. Hum. Genet., 2009, 10(1): 355-386. |
|